Trường hợp đầu tiên liên quan đến thuốc nhỏ mắt. Công ty Novartis Việt Nam xác nhận lô Tobrex 5 ml số VEE90A là hàng giả, đồng thời cảnh báo ba lô khác gồm Tobrex 5 ml (VEE98C), Maxitrol 5 ml (VFD09A) và TobraDex 5 ml (VHN07A) có dấu hiệu bị làm giả. Các sản phẩm này bị phát hiện lưu hành ngoài hệ thống phân phối chính thức.
 Văn bản từ Cục Quản lý Dược - Ảnh: Cục Quản lý Dược
Văn bản từ Cục Quản lý Dược - Ảnh: Cục Quản lý Dược
Nhóm thứ hai là thuốc ngủ liều cao Lexomil 6 mg, thuộc Công ty Cheplapharm Arzneimottel GmbH. Công an TP.HCM đã thu giữ lô F3193F01 (hạn dùng 12/2027) và được xác định là giả. Đây là lô sản xuất cho thị trường Pháp, chưa từng nhập khẩu hợp pháp vào Việt Nam. Thuốc Lexomil 6 mg cũng chưa được cấp số đăng ký lưu hành trong nước, nên mọi hoạt động mua bán đều là trái phép.
Trường hợp thứ ba liên quan đến thuốc Aclasta (acid zoledronic) điều trị loãng xương. Một nhà thuốc tại Kiên Giang phản ánh lô thuốc ghi ngày sản xuất 8/2024, hạn dùng 7/2027 có nhiều điểm bất thường. Đơn vị đăng ký khẳng định đây không phải sản phẩm nhập khẩu chính ngạch. Hơn nữa, từ sau tháng 5/2024, thuốc Aclasta chính hãng đã đổi từ logo Novartis sang Sandoz, trong khi lô này vẫn in logo cũ nên bị nghi ngờ là giả.
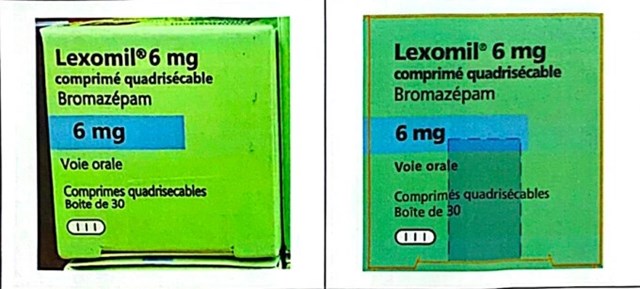 Hình ảnh so sánh giữa thuốc giả (trái) và thuốc thật (phải) do nhà sản xuất cung cấp - Ảnh: Cục Quản lý Dược
Hình ảnh so sánh giữa thuốc giả (trái) và thuốc thật (phải) do nhà sản xuất cung cấp - Ảnh: Cục Quản lý Dược
Trước thực trạng trên, Cục Quản lý Dược yêu cầu Sở Y tế các địa phương tăng cường kiểm tra, giám sát, đồng thời thông tin rộng rãi đến các cơ sở kinh doanh, bệnh viện và người dân. Người tiêu dùng được khuyến cáo chỉ mua thuốc tại cơ sở hợp pháp, kiểm tra kỹ thông tin trên bao bì, đối chiếu với dữ liệu thuốc được cấp phép trên cổng thông tin chính thức.
Cục cũng nhấn mạnh việc thực hiện nghiêm Chỉ thị 13/CT-TTg của Thủ tướng Chính phủ về chống buôn lậu, gian lận thương mại và hàng giả, cùng Kế hoạch 614/KH-BYT về phòng chống thuốc giả. Mọi dấu hiệu nghi ngờ cần báo ngay cho cơ quan chức năng để kịp thời xử lý.
LA